Контрольная
Вар - 7 в Ачинский техникум нефти и газа
600.00 руб
Дата сдачи: Март 2014
7. Современные представления о строении атома.
17. Степень окисления. Окислители и восстановители. Виды окислительно-восстановительных реакций.
27. Соединения серы: сероводород и сероводородная кислота, оксиды серы (IV и VI). Сернистая кислота и ее соли.
37. Щелочные металлы электронное строение атомов металлов, восстановительные способности, важнейшие физические и химические свойства.
47. Металлы VIII группы. Электронное строение элементов семейства железа. Общая характери¬стика. Свойства. Оксиды и гидроксиды железа. Соли железа. Применение и получение железа. Качественные реакции обнаружения ионов железа (2+ и 3+).
57. Составьте формулы соответствующих оксидов для гидроксидов: CuOH, H2SiO3, Cr(OH)3.
67. Составьте схему образования и электронные формулы следующих молекул:
N2; O2; NH3; CO2; SiF4. Укажите тип связи в этих соединениях.
77. Рассчитайте массовую долю растворенного вещества (%):
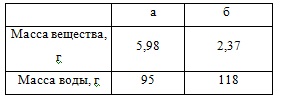
87. Как получают диоксид углерода в промышленности и лаборатории? Составьте уравнения реакций, которые надо провести, для осуществления следующих превращений: NaHCO3 CO2 CaCO3 Ca(HCO3)2.
Реакции ионного обмена запишите в молекулярно-ионном виде.
97. Составьте уравнения реакций, которые надо провести, для осуществления следующих превращений: Na2Cr2O7 Na2CrO4 Na2Cr2O7 CrCl3. Окислительно-восстановительные реакции уравняйте методом электронного баланса.
Список литературы
1. Гуров А.А., Бадаев Ф.З., Овчаренко Л.П. Химия. – М.: МГТУ им. Баумана, 2007.
2. Карапетьянц М.Х., Дракин С.И. Общая и неорганическая химия: Учебник для вузов. – М.: Химия, 1994.
3. Коровин Н. В. Общая химия. – М.: Высшая школа, 2007.
4. Угай Я.А. Общая и неорганическая химия: Учебник для вузов по напр. и спец. "Химия". – М.: Высшая школа, 1997.
Реакции ионного обмена запишите в молекулярно-ионном виде.
97. Составьте уравнения реакций, которые надо провести, для осуществления следующих превращений: Na2Cr2O7 Na2CrO4 Na2Cr2O7 CrCl3. Окислительно-восстановительные реакции уравняйте методом электронного баланса.
Список литературы
1. Гуров А.А., Бадаев Ф.З., Овчаренко Л.П. Химия. – М.: МГТУ им. Баумана, 2007.
2. Карапетьянц М.Х., Дракин С.И. Общая и неорганическая химия: Учебник для вузов. – М.: Химия, 1994.
3. Коровин Н. В. Общая химия. – М.: Высшая школа, 2007.
4. Угай Я.А. Общая и неорганическая химия: Учебник для вузов по напр. и спец. "Химия". – М.: Высшая школа, 1997.

