Контрольная
Общая и неорганическая химия Вариант 9 Контрольная работа №1
Дата сдачи: Февраль 2012
ЗАДАЧИ РЕШЕНЫ В ПИСЬМЕННОМ ВИДЕ, ПЕРЕВОД В ПЕЧАТНЫЙ ВИД НЕОБХОДИМО ОСУЩЕСТВЛЯТЬ САМОСТОЯТЕЛЬНО
1. Какова масса 1 л газовой смеси, содержащей 40% (по объёму) СО и 60% (по объёму) CO2, при температуре 27°С и давлении 2 атм?
2. Исходные концентрации NО и Cl2 в гомогенной системе 2NO + Cl2 = 2NOCl составляют соответственно 0,5 и 0,2 моль/л. Вычислите константу равновесия, если к моменту равновесия прореагировало 20% NO.
3. К 250 г 10% (по массе) раствора серной кислоты добавили 500 г раствора этой же кислоты. Определите процентную концентрацию (по массе) добавленного раствора, если образовался 3 М раствор с плотностью 1,178 г/мл.
4. Оцените реакцию среды (рН < 7, рН > 7, рН = 7) водных растворов следующих солей: ацетата свинца (II), дигидроарсената аммония, иодида калия. Напишите уравнения реакций в ионном и молекулярном виде.
5. В каком соотношении надо смешать два раствора NaOH, концентрации которых 10-2 и 10-4 М, чтобы получить раствор с рН 11?
6. Сравните рН водных растворов следующих солей:
а) арсената натрия и арсенита натрия;
б) хлорида олова (II) и хлорида олова (IV);
в) гидросульфита калия и сульфита калия.
Напишите уравнение реакции гидролиза соли, водный раствор которой имеет большее значение рН. Ответ аргументируйте сопоставлением ступенчатых констант ионизации соответствующих кислот и оснований.
7. Назовите следующие комплексные соединения, определите степень окисления и координационное число комплексообразователя, дентатность лигандов:
[Co(NH3)4(H2O)Br](NO3)2, K[La(CO3)2].
[Cu(C2H8N2)2][PtBr4];
где C2H8N2 - нейтральный лиганд этилендиамин.
Напишите выражение для константы нестойкости по второй ступени для комплексного соединения K[La(CO3)2].8. К раствору галогенида натрия добавили 10 мл 0,1 М раствора нитрата серебра. Масса образовавшегося осадка составила 0,235 г. Определите формулу галогенида.
9. Изобразите с помощью электронно-структурных схем атомов два электрона, которые:
а) находятся на одном и том же энергетическом уровне и подуровне и имеют одинаковые спины;
б) находятся на одном и том же энергетическом подуровне и имеют одинаковое значение магнитного квантового числа и одинаковые спины;
в) находятся на одном и том же энергетическом уровне и имеют одинаковое значение магнитного, квантового числа и одинаковые спины.
Используя принцип Паули, покажите, какие квантовые числа различаются у данных электронов.
10. Чтобы усилить гидролиз водного раствора сульфида натрия, необходимо:
• добавить воды;
• повысить температуру;
• понизить температуру;
• добавить гидроксида натрия;
• добавить соляную кислоту.11. Эбулиоскопическая постоянная:
• не зависит от природы растворенного вещества;
• зависит от природы растворенного вещества,
• зависит от концентрации раствора;
• зависит от природы растворителя.
12. При растворении в воде фтороводорода вода, согласно протолитической теории, выполняет функцию:
• амфолита;
• основания;
• кислоты.
13. Математическая запись закона действующих масс при химическом равновесии для реакции Н2(г) + Cl2(г) = 2HCl(r)
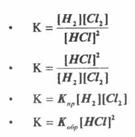
14 Уравнение Шредингера:
• не имеет решения;
• имеет бесконечное множество решений;
• имеет одно решение;
• имеет решение для атома водорода.

