Контрольная
Аналитическая химия Вариант 13 Контрольная работа 3, АГМУ
Дата сдачи: Ноябрь 2010
1. Электронные спектры поглощения. В каких координатах можно представить спектр поглощения? ЗАДАЧА. Бесцветный раствор фенолфталенина имеет спектр поглощения с максимумом при 233 нм, а на спектре фенолфталеина в щелочном растворе появляется дополнительный максимум при длине волны 553 нм. Объясните происхождение второго максимума на спектре щелочного раствора фенолфталеина. Относится ли описанное явление к какому-либо виду сдвигов или эффектов в спектре поглощения?
2. Математическое выражение закона Бугера-Ламберта-Бера. Характеристика величин в законе Бугера-Ламберта-Бера. ЗАДАЧА. Пользуясь данными таблицы, рассчитайте недостающую (отмечена знаком ?) в ней величину:
|
Оптическая плотность |
Молярный коэффициент поглощения |
Толщина слоя, см |
Концентрация |
|
0,15 |
? |
1 |
0,5 мг/250 мл М=63 г/моль |
3. Использование оптических абсорбционных методов в качественном анализе. Критерии подлинности вещества. Выберите фармакопейные методы из рассмотренных оптических методов. ЗАДАЧА. Молярный коэффициент поглощения комплекса [Fe(SCN)]2+ равен при 580 нм 7*103 л/(см*моль). Рассчитайте пропускание в процентах 2,5*10-5 моль/л раствора комплекса, измеренное при 580 нм в кювете длиной 1,00 см.
4. Выбор аналитической длины волны. Условия проведения и требования к фотометрической реакции. ЗАДАЧА. Фотоэлектроколориметр снабжён светофильтром синего цвета. Предложите пример неорганического соединения, не поглощающего в данной области спектра, определение которого можно провести с использованием фотометрической реакции.
5. Определение концентрации определяемого вещества в фотометрии. Выберите методы определения концентрации, если:
- наблюдаются отклонения от закона Бугера-Ламберта-Бера;
- оптическую плотность раствора измеряли на фотоэлектроколориметре;
- в исследуемом растворе присутствуют примеси, влияющие на величину оптической плотности («третьи компоненты»).
6. Перекисные соединения титана и ванадия при длине волны 432 нм интенсивно поглощают свет, а при длине волны 619 нм поглощает практически только ванадий. Для построения градуировочного графика приготовили стандартные растворы перекисных соединений титана и ванадия и фотометрировали их при двух длинах волн. Результаты представлены в таблице:
|
Концентрация, мг/мл |
Оптическая плотность | ||
|
Ванадий (432 нм) |
Титан (432 нм) |
Ванадий (619 нм) | |
|
0,2 |
0,36 |
0,51 |
0,16 |
|
0,4 |
0,68 |
1,10 |
0,28 |
|
0,5 |
0,83 |
1,40 |
0,34 |
|
0,6 |
1,00 |
1,68 |
0,4 |
В аналогичных условиях оптическая плотность раствора, приготовленного из исследуемого в мерной колбе на 100,00 мл, составляет 1,54 и 0,20 при длинах волн 432 и 619 нм соответственно. Определите массу (г) ванадия и титана в исследуемом растворе графическим способом.
7. Классификация электрохимических методов анализа:
- основанная на учёте природы источника электрической энергии в системе;
- по способу применения.
Сравните электрохимические методы титрования (потенциометрическое, кулонометрическое при постоянной силе тока, кондуктометрическое, биамперометрическое) по следующим параметрам:
- способы индикации точки эквивалентности;
- тип реакции в основе титрования;
- необходимость стандартизации титранта.
8. Предложите электрометрическую ячейку для количественного определения карбонат-ионов методом прямой потенциометрии, если имеется серебряный электрод. Предложите электрод сравнения. Составьте уравнение, связывающее рСО3 с потенциалом ячейки, если индикаторный электрод является катодом, а потенциал жидкостного соединения равен 0. Е0Ag2CO3/Ag = 0,46В.
9. Заполните данную таблицу:
|
Вид хроматографии |
Фазы |
Механизм разделения фаз |
Техника проведения эксперимента | |
|
ПФ |
НФ | |||
|
Жидко-жидкостная |
|
|
|
|
|
Газо-адсорбционная |
|
|
|
|
|
Ситовая |
|
|
|
|
|
Осадочная |
|
|
|
|
|
Высокоэффективная жидкостная |
|
|
|
|
10. Предложена следующая методика определения витамина в препарате: из 0,01 г (точная навеска) растёртых таблеток витамина после соответствующей обработки получают 100 мл раствора. 1 мл данного раствора снова разбавляют до 100 мл водой. Из полученного раствора отбирают аликвоту 1 мл и после дополнительных операций с последующей экстракцией витамина бутанолом получают испытуемый бутанольный экстракт, для которого измеряют интенсивность флуоресценции. В тех же условиях проводят измерение интенсивности флуоресценции стандартного раствора, содержащего 0,001 мг витамина в 1 мл.
Выведите следующую формулу для расчёта массы Х (г) витамина в одной таблетке массой 0,25 г:
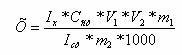
Какими объёмами и массами в методике соответствуют V1, V2, m1, m2? Назовите метод количественного определения и способ расчёта массы витамина.

