Контрольная
Аналитическая химия, контрольная №3, вариант 6 в Алтайском ГМУ
Дата сдачи: Февраль 2011
Ответы на некоторые вопросы представлены в графическом виде. Перевод в письменный вид необходимо осуществлять самостоятельно.
Инструментальные методы анализа
1. Фармакопейные методы в ФХМА. Основные способы определения концентрации в инструментальных методах анализа. Сущность метода градуировочного графика и метода добавок. Перечислите не менее четырех ИМА, использующих данные способы расчета концентрации.
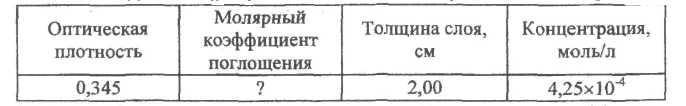
2. Закон Бугера-Ламберта-Бера. Характеристика величин в законе Бугера-Ламберта-Бера. Задача. Пользуясь данными таблицы, рассчитайте недостающую (отмечена знаком «?») в ней величину:
3. Выведите формулу, связывающую молярный и удельный коэффициент поглощения 10×ε = Е1%1см×М. Физический смысл коэффициентов ε и Е1%1см Задача. Удельный коэффициент поглощения комплекса железа (П) с фенантролином в пересчете на катионы Fe2+ при 508 нм равен 1988. Рассчитайте оптимальную молярную концентрацию данного комплекса, определяемую фотометрически в кювете длиной 1,00 см, при которой относительная систематическая ошибка фотометрического определения Fe2+ будет наименьшей.
4. Способы измерения интенсивности светового потока, прошедшего через анализируемое вещество, в адсорбционных методах анализа. Принципиальная схема и основные узлы приборов абсорбционной спектроскопии в УВИ-области спектра. Выберите источник излучения, детектор, монохроматор или светофильтр для проведения спектрофотометрического определения титана, если продукт фотометрической реакции титана с водорода пероксидом имеет максимум поглощения при длине волны 410 нм.
5. Спектр флуоресценции. Связь между спектром флуоресценции и спектром поглощения вещества. Предложите схематическое изображение спектра флуоресценции и спектра поглощения, представленных в шкале: а.) длин волн; б.) частот. С помощью данных схем проиллюстрируйте закон Стокса-Ломмела, правило зеркальной симметрии. Зависит ли вид спектра флуоресценции от длины волны возбуждающего излучения?
6. Оптические плотности стандартных растворов кислотного красного и кислотного синего, содержащих 0,0600 мг/мл красителя, измерили в кювете с толщиной слоя 1,00 см при длине волны Аэфф 500 нм и Xэфф 440 нм и получили следующие значения:

Вычислите концентрацию в г/л раствора смеси красителей, если после разбавления 10,00 мл этого раствора водой в мерной колбе на 100,00 мл и доведения до метки оптическая плотность полученного раствора, измеренная в кювете с толщиной слоя 1,00 см, при 500 нм равна 0,53, а при 440 нм равна 0,72.
7. Охарактеризуйте принцип работы медного и хлорсеребряного электродов. Установите соответствие между названием электрода и его талом.

8. На сколько мВ изменится потенциал серебряного электрода, помещенного в 200 мл 0,01 моль/л раствора аммония роданида после добавления к нему 10 мл 0,02 моль/л раствора серебра нитрата? Е° AgSCN / Ag = 0,09 В
9. Катиониты. Принцип действия, классификация, их регенерация. Количественное определение электролитов методом ИОХ. Задача. 5,00 г смеси калия и натрия нитратов растворили в воде в мерной колбе на 1000,00 мл. 50,00 мл полученного раствора пропустили через катионит в Н+-форме. Выделившуюся кислоту элюировали водой и оттитровали 27,9 мл 0,1032 моль/л раствора натрия гидроксида. Установите процентный состав пробы.
10. При кондуктометрическом титровании раствора натрия сульфата с молярной концентрацией 0,05 моль/л раствором Ва(ОН)2 с молярной концентрацией 0,8 моль/л получены следующие результаты:

Постройте кривую титрования и определите объём аликвоты раствора натрия сульфата.

